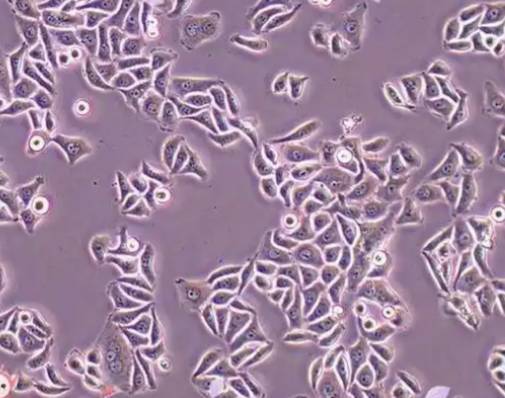
在医学研究史上,海拉细胞(HeLa Cells)堪称“永生传奇”。自1951年从美国黑人妇女海瑞塔·拉克斯的宫颈癌组织中分离以来,这种细胞以惊人的增殖能力突破了人类细胞分裂的极限——它们能在实验室培养基中无限分裂,至今已繁衍超过5000万吨,体积相当于100多幢纽约帝国大厦。然而,这种“不死”特性也引发了一个关键问题:海拉细胞能否被杀死?答案并非简单的是或否,而是需要从科学机制、实验干预与伦理边界三个维度展开探讨。
一、科学视角:海拉细胞的“不死”本质与致命弱点
海拉细胞的永生性源于其独特的生物学特性。正常人类细胞受“海弗利克上限”制约,分裂约56次后因端粒缩短而衰老死亡;而海拉细胞因感染人类乳头瘤病毒(HPV-18),其基因组整合了病毒端粒酶基因,能持续修复端粒,使细胞跳过衰老程序,实现无限增殖。此外,海拉细胞染色体数目异常(76-80条),代谢活跃,对环境适应力极强,这些特性共同构成了其“不死”的生物学基础。
然而,“不死”并不等同于不可摧毁。实验室中,科学家可通过多种手段终止海拉细胞的生命:
物理灭杀:高温(如56℃以上)、强酸强碱、紫外线辐射或机械研磨可直接破坏细胞结构,导致其死亡。
化学干预:特定化学物质(如乙醇、甲醛)可凝固细胞蛋白,阻断代谢活动;抗癌药物(如顺铂、紫杉醇)通过干扰DNA复制或微管功能诱导细胞凋亡。
生物攻击:病毒(如腺病毒、疱疹病毒)可感染海拉细胞,利用其复制机制摧毁宿主;免疫细胞(如NK细胞、T细胞)在体外实验中也能通过释放穿孔素和颗粒酶杀伤癌细胞。
例如,1952年脊髓灰质炎病毒疫苗研发中,科学家正是通过观察病毒在海拉细胞中的复制与致死过程,才成功筛选出减毒疫苗株。这一案例证明,海拉细胞虽能抵抗自然衰老,却无法逃脱定向干预下的死亡命运。
二、实验应用:从“工具细胞”到“死亡模型”
海拉细胞的“可杀性”使其成为癌症研究的重要工具。科学家通过模拟不同致死条件,揭示癌细胞的生存机制与药物作用靶点:
药物筛选:海拉细胞被广泛用于测试化疗药物的疗效。例如,研究人员发现,阿斯巴甜(无糖可乐甜味剂)可通过抑制抑癌基因表达,减缓海拉细胞凋亡并促进增殖,这一发现为评估食品添加剂致癌性提供了实验依据。
放射治疗研究:海拉细胞对X射线、γ射线敏感,科学家通过测量辐射后细胞存活率,优化癌症放疗剂量方案。
病毒学研究:海拉细胞对多种病毒易感,包括HPV、HIV、埃博拉病毒等。通过观察病毒入侵后的细胞死亡过程,科学家开发出抗病毒药物与疫苗。例如,1984年德国病毒学家利用海拉细胞证明HPV与宫颈癌的因果关系,为HPV疫苗问世奠定基础。
这些研究不仅依赖海拉细胞的“可杀性”,更凸显其作为“死亡模型”的价值——通过人为干预终止其生命,人类得以探索生命与死亡的边界,为攻克癌症提供关键线索。
三、伦理边界:从“匿名牺牲”到“尊严重构”
海拉细胞的“可杀性”讨论,无法回避其背后的伦理争议。1951年,海瑞塔·拉克斯在未被告知的情况下,其癌组织被用于细胞培养,此后数十年间,她的家人既不知情也未从相关商业收益中获益。这种“匿名牺牲”引发了全球对生物样本使用的伦理反思:
知情同意权:2013年,科学家未经许可公布海拉细胞基因组数据,可能泄露拉克斯后代的遗传信息,再次引发争议。此后,医学界逐步建立规范,要求样本使用需获捐赠者或家属明确授权。
利益共享机制:世界卫生组织(WHO)等机构呼吁,基于人体组织的研究成果应惠及捐赠者社区。例如,HPV疫苗的普及已预防超过65万例死亡,这一成果可视为对海瑞塔·拉克斯的间接致敬。
纪念与尊重:2010年,莫尔豪斯医科大学为拉克斯树立墓碑,镌刻“她的细胞,将永远造福于人类”;2021年,WHO授予其家属伦理贡献奖,承认海拉细胞对全球健康的深远影响。
这些举措表明,科学界正从“利用细胞”转向“尊重生命”——即使海拉细胞可被杀死,其来源者的尊严与权利必须被永恒守护。
结语:死亡与永生的辩证法
海拉细胞的命运,是科学探索与生命伦理交织的缩影。从生物学角度看,它们可被物理、化学或生物手段杀死,其“不死”特性仅存在于特定实验条件下;从应用价值看,它们的“可杀性”为癌症研究提供了不可替代的工具;从伦理维度看,它们的存在时刻提醒人类:科学进步不能以牺牲个体尊严为代价。
海瑞塔·拉克斯的故事,最终指向一个深刻命题:生命的价值不在于其能否被终结,而在于它如何被铭记与尊重。正如拉克斯墓碑上的铭文,海拉细胞的“永生”不仅体现在实验室的培养皿中,更体现在它们为人类健康做出的永恒贡献里。